Strategie di prevenzione e formazione professionale per la gestione dell’allevamento suinicolo in biosicurezza. È stato questo il main topic dell’incontro tenutosi dei giorni scorsi all’interno della moderna cornice del Polo universitario Veterinario di Lodi.
Nel contesto di Campus One Health si è svolto un momento di confronto tra studenti, specializzandi e medici veterinari liberi professionisti nel campo della suinicoltura con professori universitari esperti in epidemiologia veterinaria e malattie infettive degli animali domestici, nonché di biosicurezza. Il corretto uso di antimicrobici non è stato trattato solo sotto l’aspetto economico e veterinario, bensì è stato inserito nel concetto di “One Health”, salute unica, approfondendo anche l’aspetto della possibilità di trasmissione delle antibioticoresistenze anche ai germi patogeni nell’uomo. Un interessante apporto a riguardo è stato offerto dall’esperienza di Piero Marone, direttore della Uoc Microbiologia e Virologia - Fondazione Irccs Policlinico San Matteo – Pavia.
L’epidemiologia dell’antibiotico resistenza

«L’antibioticoresistenza – spiega Vittorio Sala, ordinario di Malattie Infettive degli Animali Domestici Dipartimento di Medicina veterinaria (Dimevet) - Università degli Studi di Milano - è un problema epidemiologico!».
Attraverso un excursus storico Sala fa notare che non sussistevano queste grandi preoccupazioni quando l’allevamento del suino era di tipo estensivo. Allora le terapie erano utilizzate solo in caso di estrema necessità e la prevenzione era data dall’igiene zootecnica. In quel contesto le malattie si presentavano in forme acute e ad alta mortalità.
Il grosso problema è emerso, e si è amplificato, con l’allevamento intensivo; in questo gli animali “prestazionali” crescono in tempi molto rapidi, aumentando la recettività per i patogeni (nuovi o modificati) con forme cliniche di malattia a minor mortalità rispetto al passato ma che comportano molto più impegno veterinario e di manodopera, inoltre provocano un danno economico per la minor produzione.
Il professore pone l’accento sul fatto che dapprima si siano aumentati i dosaggi e i tempi di somministrazione per poi passare all’uso auxinico (promotore della crescita) e in metafilassi (uso preventivo sull’intero gruppo di animali) degli antibiotici.
Queste metodiche indiscriminate, usate negli anni hanno indotto a un aumento rilevante dei costi sanitari, al problema dei residui ambientali e alla selezione di germi resistenti a diverse classi di antimicrobici. Siamo quindi in pieno contesto One Health dove la salute delle persone, degli animali e degli ecosistemi sono connessi.
I batteri sono stati in grado di evadere i nostri tentativi di limitarne l’impatto. La pressione selettiva data dall’ingente uso di farmaci ha permesso che solo i germi con meccanismi di difesa verso gli antibiotici sopravvivessero dopo l’effetto del medicinale. Questi stessi microbi resistenti sono riusciti a scambiare le informazioni genetiche utili con altri batteri, commensali o patogeni, con i quali sono entrati in contatto. La presenza ubiquitaria, la velocità di moltiplicazione e le modalità di scambio genico dei batteri ci hanno condotto alla presenza di innumerevoli germi patogeni multi resistenti sia in ambito zootecnico che umano.
Le conseguenze dell’errata gestione
La selezione di popolazioni resistenti è dunque riconducibile a fattori intrinseci dei microorganismi uniti alla erronea gestione del farmaco. Questa ultima componente è sostenuta da fattori di amplificazione quali:
- criteri errati di scelta del principio attivo ovvero l’uso di antibiotici non specifici per quel particolare batterio;
- eccesso e ripetitività dei trattamenti, soprattutto per via ingestiva, infatti questa via di somministrazione provoca una pressione selettiva da contatto prolungato e ripetuto tra flora enterica e antibiotico;
- incompletezza dello schema posologico considerando che solitamente la somministrazione del farmaco viene interrotta precocemente, alla remissione clinica dei sintomi che, non sempre, coincide con la guarigione (che avviene quando il sistema immunitario dell’animale è venuto a capo della moltiplicazione del batterio);
- trattamento delle infezioni opportuniste silenti, cioè trattiamo tutti i batteri che l’animale alberga, non solo i patogeni che causano la malattia in quel momento.
A fronte di tutto questo si è sviluppato il concetto di “resistoma” inteso come l’insieme di tutti i geni della resistenza agli antibiotici e dei loro precursori che all’interno dell’animale, nella sua flora microbica (saprofita, commensale e patogena), si sviluppa e può passare da una specie batterica all’altra. Lo potremmo definire una “banca dei geni della resistenza” sempre in evoluzione.
Da uno studio (Munk et al,2018) di sequenziamento metagenomico sulle feci di suini provenienti da 180 allevamenti situati in 9 diversi Paesi sono stati riscontrati 400 geni di antimicrobico resistenza. L’allevamento suinicolo intensivo è potenzialmente il bacino di incontro e scambio di resistenza in microrganismi non solo dei suini ma anche dell’uomo, di altri mammiferi (cani, gatti, roditori) e insetti.
A questo riguardo interessante diventa l’apporto delle larve di mosche sui liquami, il loro sistema enterico può diventare il fattore di amplificazione di resistenze negli allevamento e negli allevamenti vicini (Wang et al, 2017).
Di fatto non dobbiamo più considerare una epidemiologia aziendale ma una epidemiologia territoriale e di sistema produttivo dell’antibioticoresistenza in cui le mosche sono una componente molto importante.
Epidemiologia interspecie dell’antimicrobicoresistenza
Il passaggio di specie, dal suino all’uomo, per l’antibiotico resistenza può avvenire a tre livelli: con contatto diretto occupazionale, sul territorio attraverso i liquami e gli effluenti e infine al macello con le carni e i derivati. C’è una progressiva diminuzione del rischio in questo elenco, in quanto negli alimenti di origine animale si riscontrano solo i batteri di zoonosi food borne. Pertanto risulta essere il livello meno epidemiologicamente rilevante dato che i veterinari impegnati in suinicoltura stanno lavorando molto bene per ridurne l’incidenza di queste zoonosi e di conseguenza stanno abbassando il rischio di passaggio di antibiotico resistenza per questa via.
Il paradigma è lo Staphilococco aureus meticillino resistente (Mrsa) storicamente inquadrato epidemiologicamente a seconda degli ambiti di comparsa: ospedaliero, comunità umane e allevamenti. Ma inquadrarlo secondo questi tre livelli di selezione, con le conoscenze odierne è riduttivo perché non ci sono così nette separazioni e tutti posso entrare in un unico modello epidemiologico nel quale gli ambiti, attraverso le persone, si mescolano. Si tratta, attualmente, di un problema interspecifico e territoriale.
Gli studi su Mrsa presentati da Sala hanno portato alla stesura di un tipo di modello epidemiologico in cui lo Staphilococco sviluppa la resistenza nella colonizzazione nasale del suino, entra poi in contatto con le categorie esposte (allevatori, veterinari, macellatori, trasportatori, ecc.).
Non essendo specie specifico questo batterio circola ed alberga in queste persone con localizzazione nasale, e le usa come diffusori in altre comunità umane entrando in ambiti di popolazione non occupazionalmente esposta (De Faveri et al, 2014).
L’importanza di questi modelli epidemiologici nella salute pubblica ci mette di fronte alla problematica della eccessiva terapia antimicrobica sia in veterinaria che in medicina umana, in entrambi i casi è necessario un uso di antibiotico più accurato e prudente.
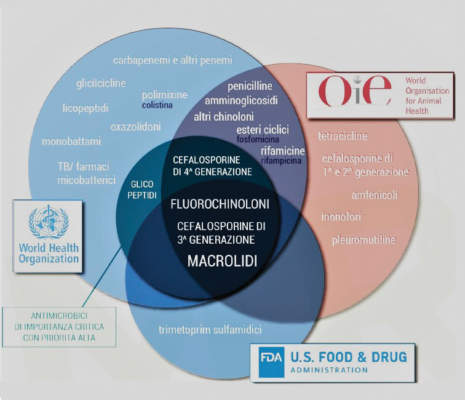
Pertanto le organizzazioni che a livello internazionale si occupano di medicina (Oie, Who, Fda) hanno proposto linee guida sull’uso degli antimicrobici, con la definizione dei Cia, cioè di principi attivi critici il cui uso va sempre più limitato.
La prospettiva futura è una sempre minor disponibilità di principi attivi da utilizzare negli animali e la non immissione sul mercato veterinario di nuove molecole, per preservarne il maggior numero dalla antimicrobico resistenza e riservarle alla medicina umana.
Infezioni correlate all’assistenza
A conferma di quanto affermato dal comparto veterinario, anche Marone afferma che infezioni correlate all’assistenza, di vario tipo e gravità, risultano spesso resistenti a diverse classi antibiotiche. L’industria farmaceutica non investe più in questo tipo di ricerca perché la capacità di trasmissione di resistenza batterica è ormai tale da rendere inefficaci in brevissimo tempo i nuovi principi attivi, rendendo rapidamente vano l’investimento fatto. Fortunatamente molecole vecchie e ormai in disuso, stanno ritornando attive perché i batteri, nella loro continua evoluzione, perdono i fattori di resistenza correlati a quelle spinte selettive non più presenti. È questo il motivo per cui, in medicina umana, sta avendo successo nel trattamento di Kleibsiella Kpc (produttrice di carbapenemati e quindi resistente ai carbapenemici) l’utilizzo di una vecchia molecola, molto nota in suinicoltura, la Colistina.
Concludendo, Marone afferma che i due problemi dell’Italia per quanto riguarda la resistenza batterica del comparto medico e ospedaliero sono paragonabili a quelli del comparto zootecnico, ovvero: l’uso non appropriato dell’antibiotico e l’insufficiente attenzione alle misure di controllo dell’infezione, che spesso sono semplici norme di igiene quali il lavaggio frequente delle mani. Per questo aspetto in medicina umana si cerca di incrementare la consapevolezza di questi fatti con campagne di prevenzione e formazione rivolte sia al personale ospedaliero sia alla popolazione. Il concetto di fondo espresso è che ognuno, nelle sue possibilità, deve fare la sua parte per salvaguardare il bene comune della salute pubblica.
La bibliografia è reperibile contattando la redazione.
Leggi l’articolo sulla Rivista di Suinicoltura n. 6/2019
Dall’edicola digitale al perché abbonarsi










